质粒DNA的提取是从事基因工程工作中的一项基本实验技术,但提取方法有很多种,以下介绍几种最常用的方法
碱裂解法
此方法适用于小量质粒DNA的提取,提取的质粒DNA可直接用于酶切、PCR扩增、银染序列分析。方法如下
1、接1%含质粒的大肠杆菌细胞于2ml LB培养基。
2、37℃振荡培养过夜。
3、取1.5ml菌体于Ep管以4000rpm离心3min,弃上清液。
4.加0.Iml溶液1(1%葡萄糖50mM/LEDTA pH8.0.25mM/L Tris-HC! pH8.0)充分混合
5、加入0.2ml溶液11(0.2 mM/L NaOH.1% SDS).轻轻翻转混匀.置于冰浴5 min。
6、加入0.15m1预冷溶液1(5 mol/L KAc.pH4.8).轻轻翻转混匀.置于冰浴5 min。
7、以10.000rpm离心20min.取上清液于另一新Ep管
8、加入等体积的异戊醇 混匀后于?0℃静置10min。
9、再以10.000rpm离心20min,弃上清。
10、用70%乙醇0.5ml洗涤一次抽干所有液体。
11、待沉淀干燥后.溶于0.05mlTE缓冲液中
煮沸法
1、将1.5ml培养液倒入eppendon管中4C下12000g离心30秒
2、弃上清.将管倒置于卫生纸上几分钟,使液体流尽。
3、将菌体沉淀悬浮于120ml STET溶液中,涡旋混匀。
4、加入10ml新配制的溶菌酶溶液(10mg/ml).涡旋振荡3秒钟。
5、将eppendon管放入沸水浴中50秒后立即取出
6、用微量离心机4℃下12000g离心10分钟
7、用无菌牙签从eppendorf管中去除细菌碎片。
8、取20ml进行电泳检查。
[注意]
1对大肠杆菌可从固体培养基上挑取单个菌落直接进行煮沸法提取质粒DNA
2.煮沸法中添加溶菌酶有一定限度.浓度高时.细菌裂解效果反而不好。有时不同溶菌酶也能溶菌,
3.提取的质粒DNA中会含有RNA但RNA并不干扰进一步实验如限制性内切酶消化.亚克隆及连接反应等。
质粒DNA的大量提取和纯化
在制作酶谱、测定序列、制备探针等实验中需要高纯度、高浓度的质粒DNA.为此需要大量提取质粒 DNA。大量提取的质粒DNA一般需进一步纯化常用柱层析法和氯化绝梯度离心法。
(一)、碱法
1、取培养至对数生长后期的含pBS质粒的细菌培养液250ml.4℃下5000g离心15分钟,弃上清,将离心管倒置使上清液全部流尽。
2、将细菌沉淀重新悬浮于50ml用冰预冷的STE中(此步可省略)。
3、同步骤1方法离心以收集细菌细胞。
4、将细菌沉淀物重新悬浮于5ml溶液|中充分悬浮菌体细胞
5、加入12ml新配制的溶液1L.盖紧瓶盖 缓缓地颠倒离心管数次以充分混匀内容物.冰浴10分钟,
6、加9ml用冰预冷的溶液I1.摇动离心管数次以混匀内容物,冰上放置15分钟,此时应形成白色絮状沉淀。
7、4C下5000g离心15分钟
8、取上清液,加入50ml RNA酶A(10mg/ml),37℃水浴20分钟。
9,加入等体积的饱和酚/氯仿 振荡混匀4℃下12000g离心10分钟
10、取上层水相.加入等体积氯仿.振荡混匀.4C下12000g离心10分钟
11、取上层水相加入1/5体积的4mol/LNaCI和10% PEG(分子量6000).冰上放置60分钟,
12、4℃下12000g离心15分钟,沉淀用数ml 70%冰冷乙醇洗涤4℃下12000g离心5分钟。
13、真空抽干沉淀.溶于500ml TE或水中。
[注意]
1.提取过程中应尽是保持低温。
2.加入溶液|和溶液川后操作应混和.切忌剧烈振荡
3.由于RNA酶A中常存在有DNA酶利用RNA酶耐热的特性.使用时应先对该酶液进行热处理(80°℃ 1小时),使DNA酶失活。
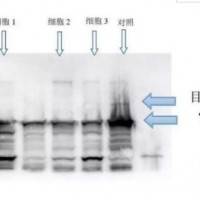
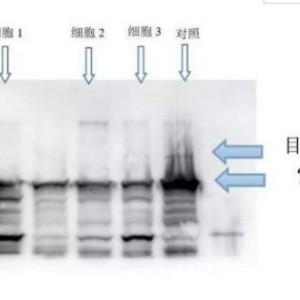
二、质粒DNA琼脂糖凝胶电泳鉴定
琼脂糖是从海藻中提取出来的一种线状高聚物.应选用电泳纯的.琼脂糖此级产品筛除了抑制物和核酸
酶.而目用溴化乙锭染色后荧光背景最小。
(1)琼脂糖凝胶电泳装置
由于琼脂糖凝胶电泳既要求不高.而适应性又强 在过去15年里已成功地设计了形形色色及大大小小的
电泳槽。对这些装置的选择主要是依据个人的喜恶。使用最普遍的装置是Walter Schaffner发明的水平板凝胶。
水平板凝胶通常在一块可安放于电泳槽平台的玻璃板或塑料盘上灌制。在有些装置中,则可将凝胶直
接铺在平台上。凝胶恰好浸在缓冲液液面下进行电泳、凝胶的电阻几平与缓冲液的电阻相同.所以有相当一部
分的电流将通过凝胶的全长。
(2)琼脂糖凝胶的制备
琼脂糖凝胶的制备是将琼脂糖在所需缓冲中液中熔化成清澈、透明的溶液。然后将熔化液倒入胶模中令其固化。凝固后,琼脂糖形成一种固体基质,其密度取决于琼脂糖的浓度。通贯凝胶的电场接通后.在中性pH值下带负电荷的DNA向阳极迁移
(3)琼脂糖凝胶的染色
电泳完毕 将琼脂糖凝胶转移入含EB的染液中染色10分钟 取出紫外灯下观察。
三、大肠秆菌感受态细胞的制备
感受态的细胞可以摄入外部溶液中的DNA.而常态的细胞却不能 所以要转化质粒DNA进入大肠杆菌必须首先制备感受态的大肠杆菌细胞。
1、取1%大肠杆菌E.coli接种于含2ml LB培养基的试管中37C振荡培养过夜
2、取0.1ml过夜培养物转种于含10ml LB培养基的三角瓶中37C振荡培养3h至OD600=0.3
3、然后把培养物倒入1.5ml离心管中冰浴10min
4、在4℃下以4000rpm离心5min,去上清液
5、把菌体悬浮于15m1冰冷的0.1M CaC12溶液中 置冰上30min
6,然后再在4℃下以4000rpm离心10min.去上清液
7、将菌体悬浮于0.1ml CaC12溶液中冰浴放置4-12hr备用。
四、质粒DNA高频转化大肠杆菌
制备好感受杰细胞后接下来就是质粒DNA转化入大肠杆菌细胞的过程。但要注意的是感受态细胞最
好是新制备的.因为保存一定时间的感受态细胞会使转化率降低此外DNA的浓度也要注意.不能太高。
1、取新制备的一管感受态细胞。
2、取0.03ml感受态细胞转和4ng质粒DNA混匀,置冰浴30min
3、将 Ep管置于42℃水浴中热冲击2分钟 立即置于冰上1分钟
4、在 Ep管中加70u1 LB培养基混匀.37C培养30min
5、涂在含话当浓度抗生素的LB平板上。
6、37℃培养过夜,长出的菌斑既为阳性克隆
五、线形质粒DNA5-粘性末端去磷酸
经限制性内切酶酶切的质粒DNA5端均带有磷酸集团.如用此载体直接转化大肠杆菌,其自身环化几率非常高.影响连接、转化效率。因此一般酶切的质粒DNA要经脱磷使用碱性磷酸酶(CIAP)去除5端磷酸集团。方法如下:
1、质粒DNA和CIAP以及BUFFER 37℃水浴30min
2、补充CIAP 再37℃水浴30min
3、加入50mM EDTA至终浓度5mM 75℃加热10min 失活CIAP
4、冷却至室温酚-氯仿抽提 乙醇沉淀浓缩。
5、抽干溶液 加适量TE溶解。